Inhaltsverzeichnis
Du möchtest wissen wie das Experiment Korrosion Handwärmer funktioniert? Hier erfährst du alles zum Experiment Korrosion Handwärmer.
Gut vermischen und einen lockeren Haufen bilden, anschließend luftdicht in einen Plastikbeutel geben und nach dem Abkühlen den Plastikbeutel öffnen (Sauerstoffzugabe).
Nachdem der Plastikbeutel geschlossen wurde (keine Sauerstoffzugabe mehr) nahm die Temperatur ab. Nach Öffnen des Beutels stieg die Temperatur bis auf ca. 75 °C an und gab diese über einen längeren Zeitraum ab. Die Farbe des Gemisches änderte sich im Laufe der Zeit von vorher schwarz/grau auf braun (Rost).
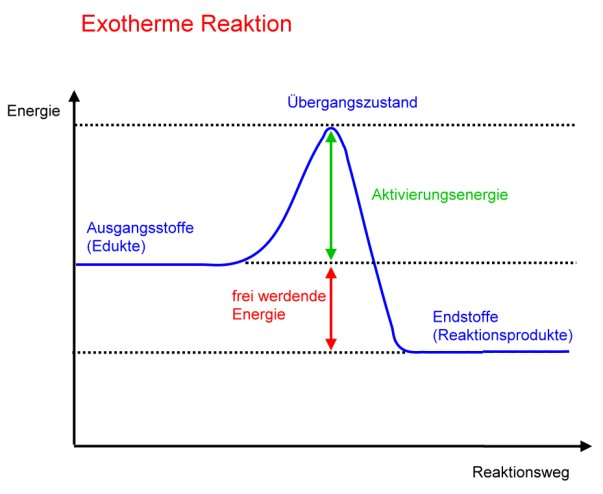
Nach Öffnen des luftdichten Plastikbeutels erfolgt eine langsame Oxidation des Eisens mit Luftsauerstoff. Durch die Verbindung mit Sauerstoff oxidiert das Eisen im Rahmen einer exothermen Reaktion, die freiwerdende Reaktionswärme wird an die Umgebung abgegeben
4 Fe + 3 O2 + 6 H2O ———> 4 Fe(OH)3
Eisen: unedles Metall welches mit Sauerstoff oxidiert
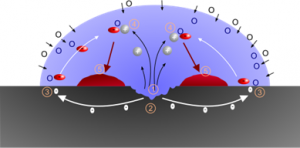
Kochsalz (NaCl): Kochsalz ist ein Elektrolyt, das Ionenwanderungen und Elektronenübergänge unterstützt. Es erhöht die Leitfähigkeit des Wassers und beschleunigt somit auch den Rostprozess
Wasser: Lösungsmittel, sowie katalytische Aufgaben
Aktivkohle: Die Aktivkohle wirkt katalytisch, denn diese „saugt“ den Sauerstoff an, aktiviert ihn und reicht ihn an das Eisen weiter. Dadurch wird die Reaktionsgeschwindigkeit erhöht und der Rostprozess beschleunigt. Außerdem hält diese die Eisenteilchen auf Abstand und erleichtert so den Gas-Austausch. Es dient zusätzlich auch als Wasserspeicher.
Sauerstoff: Oxidationsmittel (nimmt Elektronen auf)