
Eine endotherme Reaktion ist eine chemische Reaktion, bei der Energie aufgenommen wird. Das bedeutet, dass die Reaktion Energie in Form von Wärme aufnimmt, wodurch sich die Temperatur verringert.
Endotherme Reaktionen treten häufig in der Natur auf und können auch in Laboratorien oder Industrieanlagen beobachtet werden. Ein Beispiel für eine endotherme Reaktion ist die Verdunstung von Wasser, bei der Wärme aufgenommen wird, um die Moleküle von der flüssigen in die gasförmige Phase zu bringen.
Endotherme Reaktionen können auch in der Medizin verwendet werden, zum Beispiel bei der Herstellung von Medikamenten oder bei der Kühlung von Geweben.
Es ist wichtig zu beachten, dass endotherme Reaktionen möglicherweise nicht immer ungefährlich sind und dass bestimmte Vorkehrungen getroffen werden müssen, um sicherzustellen, dass sie sicher ablaufen. Zum Beispiel kann es bei manchen endothermen Reaktionen zu Explosionen oder Bränden kommen, wenn sie nicht sorgfältig kontrolliert werden.
Ein Energiediagramm ist eine grafische Darstellung der Energieveränderungen, die während einer chemischen Reaktion stattfinden. Es zeigt die Energie der beteiligten Moleküle und Atome zu verschiedenen Zeitpunkten während der Reaktion.
Ein Energiediagramm für eine endotherme Reaktion zeigt, dass die Energie der beteiligten Moleküle und Atome während der Reaktion zunimmt. Das bedeutet, dass die Energie der Produkte der Reaktion höher ist als die Energie der Ausgangsstoffe. Die Differenz zwischen den beiden Energien wird als Freie Enthalpie der Reaktion bezeichnet und ist ein Maß dafür, wie viel Energie aufgenommen wurde.
Ein Energiediagramm für eine endotherme Reaktion sieht in etwa so aus:
Ausgangsstoffe -> Übergangszustand -> Produkte
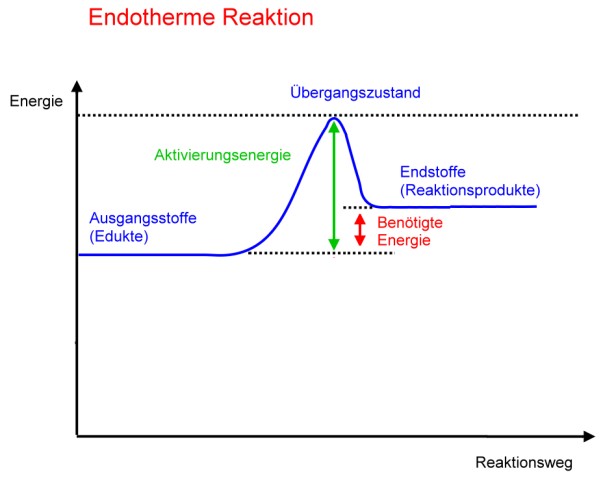
Die Linie auf dem Diagramm zeigt die Energieveränderung während der Reaktion. Sie verläuft von unten nach oben, da die Energie während der Reaktion zunimmt.
Es ist wichtig zu beachten, dass Energiediagramme nur ein grobes Bild der Energieveränderungen während einer Reaktion liefern und dass es in der Praxis oft komplizierter ist. Es gibt viele Faktoren, die die Energieveränderungen während einer Reaktion beeinflussen können, wie zum Beispiel die Temperatur, der Druck und die Konzentration der beteiligten Substanzen.
